肺がんにおける術後アジュバントosimertinib:DFS延長の意義は?
以前に、「術後アジュバントosimertinib治療に賛成?反対?」というテーマで記事を書いた。(リンクはこちら)
実際の承認や、さらなるデータの蓄積なしには詳細な議論に限界があるが、前回の記事から4か月経った今、前回の内容も振り返りながらADAURAの使用について再考したい。
ADAURAは、術後アジュバントとしてのosimertinibが、無病生存期間(DFS)を大幅に延長することが示されたポジティブ試験である。特に化学療法と比べると副作用も管理しやすく長期間服薬が可能であること、また高いCNS透過率による脳転移をはじめとした再発の予防に有効であることが、ADAURAのメリットとして考えられる。
一方、術後にosimertinibを使用し続けることによる医療費負担の増大や長期服薬によるAE発現、QOL低下など懸念点も多く残されている。そのため、腫瘍切除後さらなる治療が必要かどうかも分からない症例全例に、drug freeの機会を犠牲にしてまで術後osimertinibを使用するかどうかに関しては、賛否が分かれるところである。
ADAURAのメリット・デメリット・分かっていないことを図1にまとめたが、今回は特に昨今議論されることも多くなってきた、osimertinibを「どのタイミグで開始し、いつまで続けるのが最適か」という点について考えてみたい。
ADAURAで重要なのはDFS延長効果だけではない
従来の術後アジュバントTKIの治験においては比較対象が化学療法群であったのに対し、ADAURAにおいては比較対象が無治療群(placebo)である。(Liu et al. JCO 2021)また、薬剤継続期間が既報の試験で設定された2年ではなく3年であることや、進行期のosimertinibの薬効のエビデンスを考えると、medium follow-up期間が3年にも達していない現時点でDFSに差がつくことは当然とも言える。今後問題となるのは、osimertinibをいつまで続けるのか、そもそも腫瘍を切除した直後からosimertinibを使う必要があるのか、という点である。
osimertinibの最適な使い方は、術後に3年間?再発するまでまでずっと?再発後?
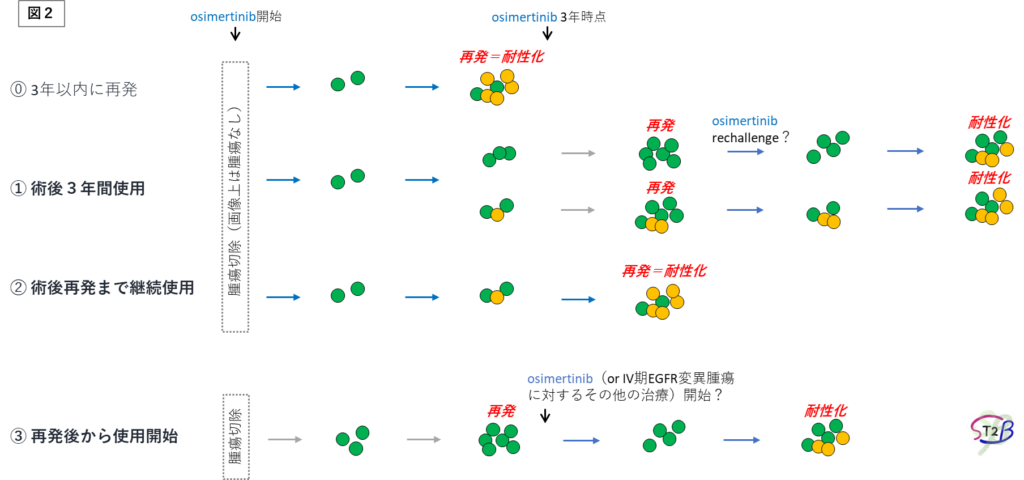
この問いに答えるために重要なのは、いかにosimertinibへの耐性化を遅らせるかということである。osimertinib耐性化のメカニズムは非常にヘテロであることが分かっており(Leonetti et al. British Journal of Cancer 2019)未だ有効な治療法が定まっていないからである。では図2とともに、osimertinibの使用パターン毎に耐性化に至る過程を考えてみたい。
早期の術後アジュバントが対象となる腫瘍はよりheterogeneityが低いと考えられ、目に見てる腫瘍は除去した状態であるため、進行期と比較して耐性化にはより時間がかかると推察される。実際FLAURAの結果ではmedian PFSが18.9か月である一方、ADAURAの結果ではmedian DFSがNot Reached(median follow-up期間22.1か月時点)であり、(追跡期間はまだ短いが)術後アジュバント治療に対する耐性化には時間がかかることが示唆される。このことから、一定数の症例に関してはosimertinibを3年間使用した時点でまだ再発に至っておらず、その時点でosimertinibを中止するかどうかにより、下図の①、➁いずれかの経過を辿ると考えられる。osimertinibを3年完遂後無治療に切り替える場合(①)、続く再発時にosimertinibのrechallengeの余地が残されている。*しかしながら、再発するまでosimertinibを続けた場合(➁)、再発とともに耐性クローンが発現して「再発=耐性化」となる可能性が高い。
では術後すぐに服薬を開始せずに再発してからosimertinibを開始する場合はどうか。③に示すとおり、確かに術後アジュバント治療を実施した場合と比較すると再発時期は早まるが、再発後すぐにosimertinibを開始することで十分な抗腫瘍効果を得ることができ、耐性化までの時間稼ぎにつながるかもしれない。 (osimertinibを開始した時点で、そこから腫瘍は耐性化への一途を辿る、そう考えると、再発するまではdrug freeで過ごし、osimertinibは再発後からスタートするという方針も個人的には捨てがたいと感じるがいかがだろうか。)
以上のことから、ADAURAのポジティブな結果を受けて術後アジュバントosimertinibに大賛成というわけにはいかず、osimertinib使用開始のタイミングや継続期間に関しても議論が一筋縄ではいかない。特に、①と③ではどちらが長期的に見てOS延長につながるか、臨床試験から答えを得ることは難しい。
我が国においてもADAURAが承認になる日は近いことが予想されるため、実臨床での使い方や患者さんへの説明に迷わないためにも、まだまだ議論を重ね、考えを深めていく必要があるだろう。
=EGFR-TKIのrechallenge=
TKI耐性EGFR変異細胞は、TKI感受性EGFR変異細胞と比べて増殖スピードが遅いとの報告があり、TKIをやめるとTKI感受性細胞が一気に増殖する。(J Chmielecki et al. Sci Transl Med. 2011)これがTKIを急に中止したときに見られるflare-upにもつながると考えられる。そのため、osimertinibを3年使用した時点でわずかな耐性クローンが生じていたとしても、osimertinibを中断することで、osimertinib感受性クローンが再増殖することが予想され、osimertinibのrechallengeが可能になると考えられる。
実際にCTONG1104の結果を見ると、術後アジュバントgefitinib治療群の中でも再発後にEGFR-TKIを使用した症例が最も長いOS延長につながったとの結果が得られている。(Zhong et al. JCO 2021)EGFR-TKIのrechallengeをしながらうまく耐性細胞をコントロールすることで、予後延長につながる戦略も悪くないかもしれない。